Speciální metodiky pro stanovení buněčných fyziologických parametrů
Měření vnitrobuněčného pH
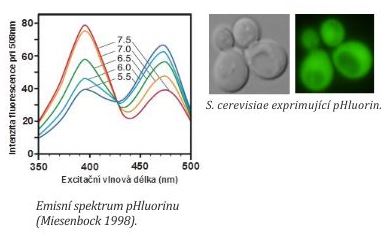
Pro měření vnitrobuněčného pH v kvasinkách využíváme pHluorin (zelený fluorescenční protein citlivý na změny pH). Gen kódující pHluorin je do buněk kvasinek vnesen na plasmidu nebo integrován do genomu. Metoda umožňuje měření pH v buňkách kvasinek za fyziologických podmínek. Princip: pHluorin má dvě excitační maxima při 395 a 475 nm. Intenzita fluorescence při těchto vlnových délkách je u pHluorinu závislá na koncentraci protonů (pH). V buňkách určíme poměr intenzit fluorescence při excitačních maximech a hodnotu pH následně odečteme z kalibrační křivky (= závislost poměru intenzit fluorescence 395 nm/475 nm v buňkách exprimujících pHluorin na pH kalibračních pufrů).
Měření vnitrobuněčných koncentrací kationtů
Při studiu vlastností a fyziologických rolí přenašečů kationtů alkalických kovů se často zajímáme, jak přítomnost, nepřítomnost nebo pozměněná struktura transportérů ovlivňuje množství kationtů v kvasince. Obsah studovaných buněk extrahujeme v roztoku kyseliny chlorovodíkové a koncentraci uvolněných kationtů stanovujeme metodou plamenové atomové absorpční spektrometrie.
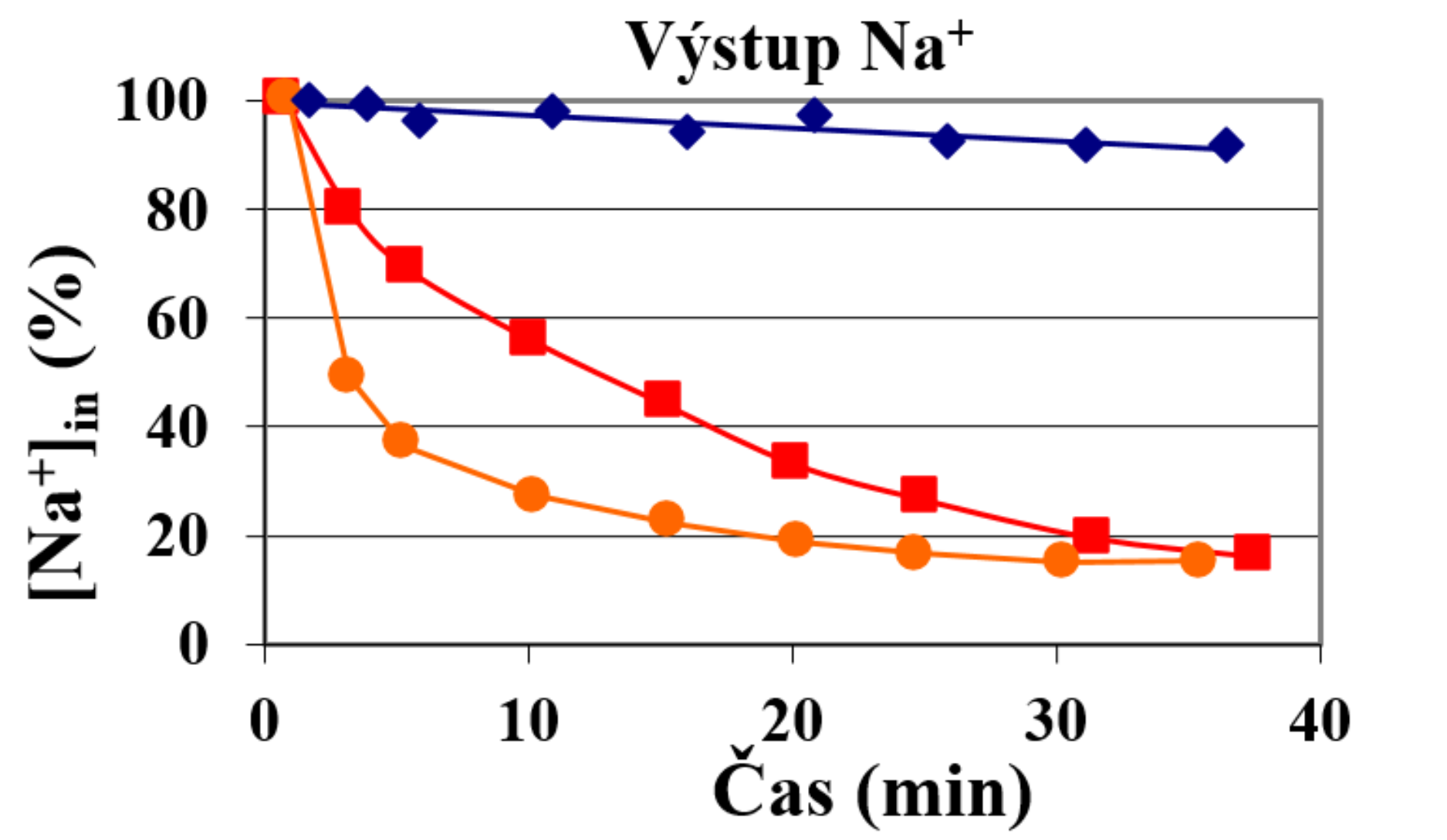
Stanovení obsahu sodných kationtů během 40 min v buňkách S. cerevisiae BW31 bez exportérů sodných kationtů (modrá ♦) nebo produkujících transportéry ScNha1p (červená ■) či YlNha2p (oranžová ●) ukazuje, že YlNha2 má vyšší aktivitu (exportuje Na+ z buněk rychleji) než ScNha1.
Membránový potenciál
Metoda měření membránového potenciálu kvasinek (Gášková et al., 1998) využívá fluorescenční sondu, poloha jejího maxima fluorescenční emise (lmax) a intenzita fluorescence v maximu (Imax) citlivě odpovídají na změny v membránovém potenciálu v suspenzi buněk. Tato kladně nabitá sonda snadno vstupuje do buněk a hromadí se uvnitř v závislosti na velikosti vnitřního záporného membránového potenciálu až do ustavení rovnováhy. V buňkách s vysokým membránovým potenciálem (hyperpolarizace membrány) se hromadí velké množství sondy, naopak menší akumulace odráží depolarizaci membrány.
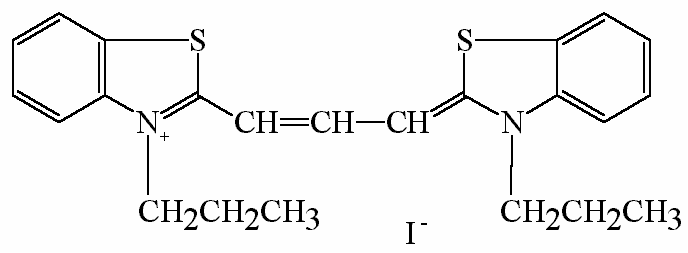
diS-C3(3) (3,3´-dipropylthiokarbocyanin jodid)
Odpověď sondy diS-C3(3) na membránový potenciál je rozhodujícím způsobem ovlivněna činností MDR pump. Sonda je z kvasinek S. cerevisiae odstraňována ABC pumpami Pdr5 a Snq2 a z kvasinek C. glabrata pumpou Cdr1, může být tudíž využita pro studium jejich činnosti a hledání jejich inhibitorů.
Princip:
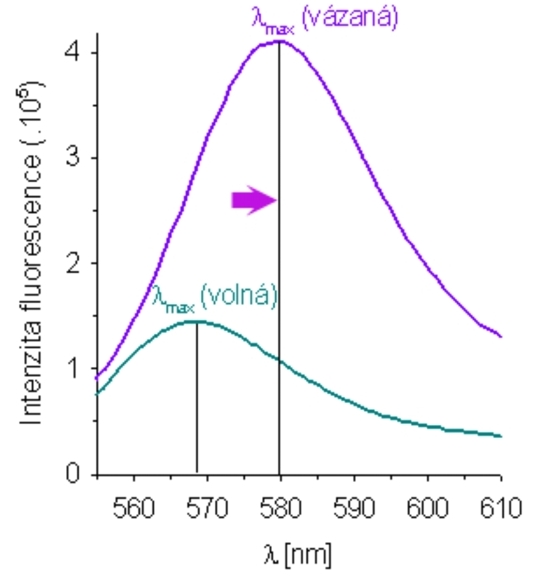
Vazba sondy diS-C3(3) na buněčné součásti je doprovázena změnami v jejích spektroskopických vlastnostech:
- maximum fluorescenční emise vázané sondy je posunuté směrem k delším vlnovým délkám přibližně o 10 nm ve srovnání s maximem emise volné sondy (569 nm)
- intenzita fluorescence značně vzroste díky prodloužení doby života a zvětšení kvantového výtěžku.
Metoda využívá sledování časového průběhu posuvů vlnové délky maximální emise po přidání fluorescenční sondy k buňkám, tzv. barvicí křivky.